MINISTERIO DE SALUD Y DESARROLLO SOCIAL
SECRETARÍA DE GOBIERNO DE SALUD
Resolución 423/2018
RESOL-2018-423-APN-SGS#MSYDS
Ciudad de Buenos Aires, 12/11/2018
VISTO el Expediente EX-2018-09284756 APN-DD#MS del registro de la SECRETARÍA DE GOBIERNO DE SALUD, la Ley Nº 23.753 y sus modificatorias, el Decreto Nº 1286 del 6 de agosto de 2014, la Decisión Administrativa N° 307 del 13 de marzo de 2018, Resolución de la ex SECRETARIA DE SALUD Nº 45 del 24 de enero de 1994, y Resolución Nº 1156 del 23 de julio de 2014, y
CONSIDERANDO:
Que por Ley Nº 23.753 se asigna competencia al entonces MINISTERIO DE SALUD DE LA NACIÓN para coordinar junto a las autoridades sanitarias de todo el país, la planificación de acciones tendientes a asegurar a las personas con diabetes los medios terapéuticos que requieran para su tratamiento así como los medios para su control evolutivo.
Que el artículo 5° de la referida norma, incorporado por la Ley Nº 26.914, dispone que la autoridad de aplicación, debe establecer las “Normas de Provisión de Medicamentos e Insumos”, las que deberán ser revisadas y actualizadas como mínimo cada dos años a fin de poder incluir en la cobertura los avances farmacológicos y tecnológicos que resulten de aplicación en la terapia y promuevan una mejora en la calidad de vida a personas con diabetes.
Que el Decreto N° 1286/2014 señala que deberán disponerse las medidas necesarias para garantizar a las personas con diabetes el aprovisionamiento de los medicamentos y reactivos de diagnóstico para autocontrol que se estimen como elementos indispensables para un tratamiento adecuado, según lo establecido por las normas técnicas aprobadas por autoridad competente en el orden nacional, y que su financiación corresponde a la Seguridad Social, a la medicina privada y, en caso de pacientes carentes de dichas coberturas, a cargo del gobierno de la jurisdicción.
Que por Resolución 1156/2014 del ex MINISTERIO DE SALUD DE LA NACIÓN aprobó la última actualización de las “NORMAS DE PROVISIÓN DE MEDICAMENTOS E INSUMOS” y el “MODELO DE CERTIFICADO PARA LA ACREDITACION DE PERSONAS CON DIABETES” que todos los Agentes del SISTEMA NACIONAL DEL SEGURO DE SALUD enmarcados en las Leyes N° 23.660 y N° 23.661, las Entidades de Medicina Prepaga (Ley N° 26.682), el INSTITUTO NACIONAL DE SERVICIOS SOCIALES PARA JUBILADOS Y PENSIONADOS (Ley N° 19.032), la OBRA SOCIAL DEL PODER JUDICIAL DE LA NACIÓN, la DIRECCION DE AYUDA SOCIAL PARA EL PERSONAL DEL CONGRESO DE LA NACIÓN, el INSTITUTO DE OBRA SOCIAL DE LAS FUERZAS ARMADAS y las OBRAS SOCIALES UNIVERSITARIAS (Ley N° 24741) pueden expedir a través de sus efectores.
Que considerando las modificaciones realizadas a la Ley Nº 23.753 a partir del dictado de la Ley Nº 26.914, la DIRECCION NACIONAL DE PROMOCION DE LA SALUD Y CONTROL DE ENFERMEDADES CRÓNICAS NO TRANSMISIBLES ha elaborado en conjunto con la COMISIÓN PERMANENTE ASESORA DE DIABETES (integrada por la Sociedad Argentina de Diabetes, la Sociedad Argentina de Nutrición, el Centro de Endocrinología Experimental y Aplicada, la Asociación de Facultades de Ciencias Médicas de la República Argentina, la Federación Argentina de Diabetes, la Liga de Protección al Diabético, la Asociación para el Cuidado de la Diabetes en Argentina y la Superintendencia de Servicios de Salud) una propuesta de actualización a las Normas de Provisión de Medicamentos e Insumos.
Que la SUBSECRETARÍA DE PROMOCIÓN DE LA SALUD Y PREVENCIÓN DE LA ENFERMEDAD, ha prestado la debida conformidad.
Que la UNIDAD DE COORDINCIÓN GENERAL, ha prestado su debida conformidad.
Que la DIRECCION GENERAL DE ASUNTOS JURIDICOS ha tomado la intervención de su competencia.
Que la presente medida se dicta en ejercicio de las facultades conferidas por el Decreto Nº 802 del 5 de Septiembre del 2018.
Por ello,
EL SECRETARIO DE GOBIERNO DE SALUD
RESUELVE:
ARTICULO 1° — Apruébase la actualización de las “NORMAS DE PROVISION DE MEDICAMENTOS E INSUMOS PARA PERSONAS CON DIABETES” que como ANEXO I (IF-2018-55919268-APN-SPSPYCR#MSYDS) forma parte de la presente.
ARTICULO 2° — Apruébase el nuevo “MODELO DE CERTIFICADO PARA LA ACREDITACION DE PERSONAS CON DIABETES” que como ANEXO II (IF-2018-55922150-APN-SPSPYCR#MSYDS) forma parte de la presente. Las Obras Sociales (Leyes Nº 23.660 y Nº 23.661),las Entidades de Medicina Prepaga (Ley Nº 26.682), el INSTITUTO NACIONAL DE SERVICIOS SOCIALES PARA JUBILADOS Y PENSIONADOS (Ley N° 19.032), la OBRA SOCIAL DEL PODER JUDICIAL DE LA NACIÓN, la DIRECCION DE AYUDA SOCIAL PARA EL PERSONAL DEL CONGRESO DE LA NACIÓN, el INSTITUTO DE OBRA SOCIAL DE LAS FUERZAS ARMADAS y las OBRAS SOCIALES UNIVERSITARIAS (Ley N° 24741) podrán, en cumplimiento de lo establecido por la Ley Nº 23.753 y sus modificatorias, y a los fines de garantizar el acceso de la cobertura y evitar barreras, expedir la certificación a través de sus efectores. La certificación referida en el párrafo precedente se hará al momento del diagnóstico. Teniendo en cuenta que la condición de enfermedad crónica no caduca, pero la terapéutica y características de la enfermedad varían en función del estado y curso evolutivo que la persona con diabetes experimente, se establece que la certificación efectuada en el momento del diagnóstico deberá ser actualizada anualmente y con menor periodicidad ante cada cambio del tratamiento.
ARTICULO 3º — Déjese sin efecto los anexos II y III de la Resolución 1156/2014 los cuales serán reemplazados por los ANEXOS I y II de la presente.
ARTÍCULO 4° - Los ANEXOS I y II de la presente resolución pasarán a integrar el Sistema de Prestaciones Médicas Obligatorias (PMO).
ARTICULO 5° — Las Obras Sociales nacionales, las Entidades de Medicina Prepaga, el INSTITUTO NACIONAL DE SERVICIOS SOCIALES PARA JUBILADOS Y PENSIONADOS, la OBRA SOCIAL DEL PODER JUDICIAL DE LA NACIÓN, la DIRECCION DE AYUDA SOCIAL PARA EL PERSONAL DEL CONGRESO DE LA NACIÓN, el INSTITUTO DE OBRA SOCIAL DE LAS FUERZAS ARMADAS y las OBRAS SOCIALES UNIVERSITARIAS deberán establecer los procedimientos administrativos necesarios a fin de garantizar la provisión de medicamentos e insumos acorde lo estipulado en el ANEXO I de la presente norma.
ARTÍCULO 6°- Invítase a las jurisdicciones provinciales y a la CIUDAD AUTONOMA DE BUENOS AIRES a instrumentar los mecanismos necesarios tendientes a garantizar la cobertura a las personas que no estén comprendidas en el Sistema Nacional de Seguro de Salud.
ARTICULO 7° — Regístrese, comuníquese, dese a la Dirección Nacional del Registro Oficial para su publicación y archívese. Adolfo Luis Rubinstein
NOTA: El/los Anexo/s que integra/n este(a) Resolución se publican en la edición web del BORA -www.boletinoficial.gob.ar-
SECRETARÍA DE GOBIERNO DE SALUD
Resolución 423/2018
RESOL-2018-423-APN-SGS#MSYDS
Ciudad de Buenos Aires, 12/11/2018
VISTO el Expediente EX-2018-09284756 APN-DD#MS del registro de la SECRETARÍA DE GOBIERNO DE SALUD, la Ley Nº 23.753 y sus modificatorias, el Decreto Nº 1286 del 6 de agosto de 2014, la Decisión Administrativa N° 307 del 13 de marzo de 2018, Resolución de la ex SECRETARIA DE SALUD Nº 45 del 24 de enero de 1994, y Resolución Nº 1156 del 23 de julio de 2014, y
CONSIDERANDO:
Que por Ley Nº 23.753 se asigna competencia al entonces MINISTERIO DE SALUD DE LA NACIÓN para coordinar junto a las autoridades sanitarias de todo el país, la planificación de acciones tendientes a asegurar a las personas con diabetes los medios terapéuticos que requieran para su tratamiento así como los medios para su control evolutivo.
Que el artículo 5° de la referida norma, incorporado por la Ley Nº 26.914, dispone que la autoridad de aplicación, debe establecer las “Normas de Provisión de Medicamentos e Insumos”, las que deberán ser revisadas y actualizadas como mínimo cada dos años a fin de poder incluir en la cobertura los avances farmacológicos y tecnológicos que resulten de aplicación en la terapia y promuevan una mejora en la calidad de vida a personas con diabetes.
Que el Decreto N° 1286/2014 señala que deberán disponerse las medidas necesarias para garantizar a las personas con diabetes el aprovisionamiento de los medicamentos y reactivos de diagnóstico para autocontrol que se estimen como elementos indispensables para un tratamiento adecuado, según lo establecido por las normas técnicas aprobadas por autoridad competente en el orden nacional, y que su financiación corresponde a la Seguridad Social, a la medicina privada y, en caso de pacientes carentes de dichas coberturas, a cargo del gobierno de la jurisdicción.
Que por Resolución 1156/2014 del ex MINISTERIO DE SALUD DE LA NACIÓN aprobó la última actualización de las “NORMAS DE PROVISIÓN DE MEDICAMENTOS E INSUMOS” y el “MODELO DE CERTIFICADO PARA LA ACREDITACION DE PERSONAS CON DIABETES” que todos los Agentes del SISTEMA NACIONAL DEL SEGURO DE SALUD enmarcados en las Leyes N° 23.660 y N° 23.661, las Entidades de Medicina Prepaga (Ley N° 26.682), el INSTITUTO NACIONAL DE SERVICIOS SOCIALES PARA JUBILADOS Y PENSIONADOS (Ley N° 19.032), la OBRA SOCIAL DEL PODER JUDICIAL DE LA NACIÓN, la DIRECCION DE AYUDA SOCIAL PARA EL PERSONAL DEL CONGRESO DE LA NACIÓN, el INSTITUTO DE OBRA SOCIAL DE LAS FUERZAS ARMADAS y las OBRAS SOCIALES UNIVERSITARIAS (Ley N° 24741) pueden expedir a través de sus efectores.
Que considerando las modificaciones realizadas a la Ley Nº 23.753 a partir del dictado de la Ley Nº 26.914, la DIRECCION NACIONAL DE PROMOCION DE LA SALUD Y CONTROL DE ENFERMEDADES CRÓNICAS NO TRANSMISIBLES ha elaborado en conjunto con la COMISIÓN PERMANENTE ASESORA DE DIABETES (integrada por la Sociedad Argentina de Diabetes, la Sociedad Argentina de Nutrición, el Centro de Endocrinología Experimental y Aplicada, la Asociación de Facultades de Ciencias Médicas de la República Argentina, la Federación Argentina de Diabetes, la Liga de Protección al Diabético, la Asociación para el Cuidado de la Diabetes en Argentina y la Superintendencia de Servicios de Salud) una propuesta de actualización a las Normas de Provisión de Medicamentos e Insumos.
Que la SUBSECRETARÍA DE PROMOCIÓN DE LA SALUD Y PREVENCIÓN DE LA ENFERMEDAD, ha prestado la debida conformidad.
Que la UNIDAD DE COORDINCIÓN GENERAL, ha prestado su debida conformidad.
Que la DIRECCION GENERAL DE ASUNTOS JURIDICOS ha tomado la intervención de su competencia.
Que la presente medida se dicta en ejercicio de las facultades conferidas por el Decreto Nº 802 del 5 de Septiembre del 2018.
Por ello,
EL SECRETARIO DE GOBIERNO DE SALUD
RESUELVE:
ARTICULO 1° — Apruébase la actualización de las “NORMAS DE PROVISION DE MEDICAMENTOS E INSUMOS PARA PERSONAS CON DIABETES” que como ANEXO I (IF-2018-55919268-APN-SPSPYCR#MSYDS) forma parte de la presente.
ARTICULO 2° — Apruébase el nuevo “MODELO DE CERTIFICADO PARA LA ACREDITACION DE PERSONAS CON DIABETES” que como ANEXO II (IF-2018-55922150-APN-SPSPYCR#MSYDS) forma parte de la presente. Las Obras Sociales (Leyes Nº 23.660 y Nº 23.661),las Entidades de Medicina Prepaga (Ley Nº 26.682), el INSTITUTO NACIONAL DE SERVICIOS SOCIALES PARA JUBILADOS Y PENSIONADOS (Ley N° 19.032), la OBRA SOCIAL DEL PODER JUDICIAL DE LA NACIÓN, la DIRECCION DE AYUDA SOCIAL PARA EL PERSONAL DEL CONGRESO DE LA NACIÓN, el INSTITUTO DE OBRA SOCIAL DE LAS FUERZAS ARMADAS y las OBRAS SOCIALES UNIVERSITARIAS (Ley N° 24741) podrán, en cumplimiento de lo establecido por la Ley Nº 23.753 y sus modificatorias, y a los fines de garantizar el acceso de la cobertura y evitar barreras, expedir la certificación a través de sus efectores. La certificación referida en el párrafo precedente se hará al momento del diagnóstico. Teniendo en cuenta que la condición de enfermedad crónica no caduca, pero la terapéutica y características de la enfermedad varían en función del estado y curso evolutivo que la persona con diabetes experimente, se establece que la certificación efectuada en el momento del diagnóstico deberá ser actualizada anualmente y con menor periodicidad ante cada cambio del tratamiento.
ARTICULO 3º — Déjese sin efecto los anexos II y III de la Resolución 1156/2014 los cuales serán reemplazados por los ANEXOS I y II de la presente.
ARTÍCULO 4° - Los ANEXOS I y II de la presente resolución pasarán a integrar el Sistema de Prestaciones Médicas Obligatorias (PMO).
ARTICULO 5° — Las Obras Sociales nacionales, las Entidades de Medicina Prepaga, el INSTITUTO NACIONAL DE SERVICIOS SOCIALES PARA JUBILADOS Y PENSIONADOS, la OBRA SOCIAL DEL PODER JUDICIAL DE LA NACIÓN, la DIRECCION DE AYUDA SOCIAL PARA EL PERSONAL DEL CONGRESO DE LA NACIÓN, el INSTITUTO DE OBRA SOCIAL DE LAS FUERZAS ARMADAS y las OBRAS SOCIALES UNIVERSITARIAS deberán establecer los procedimientos administrativos necesarios a fin de garantizar la provisión de medicamentos e insumos acorde lo estipulado en el ANEXO I de la presente norma.
ARTÍCULO 6°- Invítase a las jurisdicciones provinciales y a la CIUDAD AUTONOMA DE BUENOS AIRES a instrumentar los mecanismos necesarios tendientes a garantizar la cobertura a las personas que no estén comprendidas en el Sistema Nacional de Seguro de Salud.
ARTICULO 7° — Regístrese, comuníquese, dese a la Dirección Nacional del Registro Oficial para su publicación y archívese. Adolfo Luis Rubinstein
NOTA: El/los Anexo/s que integra/n este(a) Resolución se publican en la edición web del BORA -www.boletinoficial.gob.ar-
e. 14/11/2018 N° 86466/18 v. 14/11/2018
(Nota Infoleg: Los anexos referenciados en la presente norma han sido extraídos de la edición web de Boletín Oficial)


ANEXO I
(Anexo rectificado por art. 2° de la Resolución N° 764/2018 de la Secretaría de Gobierno de Salud B.O. 12/12/2018)
Normas de Provisión de Medicamento e Insumos para Personas con Diabetes Mellitus.
Las modificaciones a la norma precedente contenidas en este reglamento están basadas en una búsqueda exhaustiva, selección y análisis crítico de la evidencia proveniente de Guías de Práctica Clínica, revisiones sistemáticas y meta-análisis de alta calidad metodológica referentes a la temática, valorando especialmente la efectividad clínica y seguridad de las personas con diabetes.
Glosario
DM1: diabetes mellitus tipo 1
DM2: diabetes mellitus tipo 2
HbA1c: hemoglobina glicosilada A1c
IDPP4: inhibidores de la dipeptidil peptidasa 4
NPH: Neutral Protamine Hagedorn.
Aspectos relevantes de la actualización:
- Discontinuar la cobertura 100% de glibenclamida.
- Incorporar la cobertura de gliclazida.
- Excluir la cobertura de las Insulinas porcina y bovina, jeringas de insulina U40 y U80.
- Aumentar la cobertura del número de agujas para aplicación de insulina.
- Incorporar la cobertura de vildagliptina/sitagliptina, para subpoblaciones específicas.
- Incorporar la cobertura de insulinas lispro U200, glargina U300 y degludec para subpoblaciones específicas.
- Incorporar la cobertura de glucagón, para subpoblación especifica.
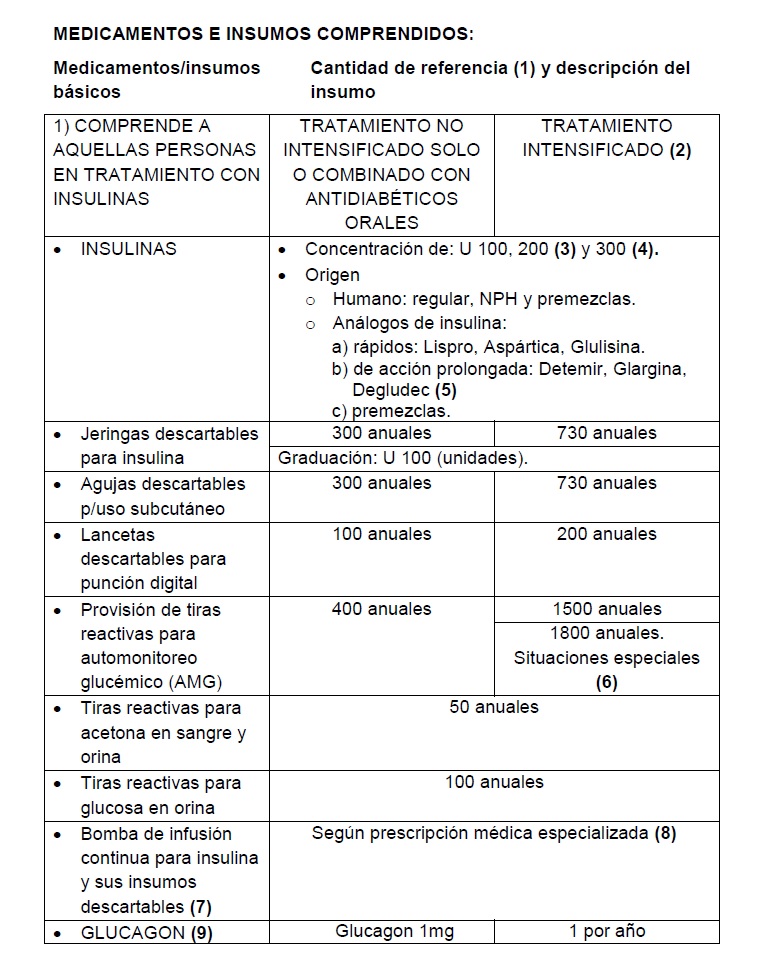

(1) Cantidades de referencia: son aquellas establecidas para dar respuesta adecuada a la gran mayoría de las personas con diabetes en los diferentes esquemas terapéuticos recomendados. Pueden ser modificadas ante casos particulares debidamente documentados mediante historia clínica y registro semanal de glucemias.
(2) Tratamiento intensificado: consiste en administración de insulina basal (NPH dos a tres veces al día, insulina detemir dos veces al día o insulina glargina/degludec, una vez al día), más insulina adicional de acción rápida en relación a las ingestas (insulina regular o análogos rápidos), o bomba de infusión continua subcutánea. El tratamiento intensificado será indicado por médico especializado (8).
(3) Insulina lispro U200: solamente si el precio por unidad de insulina lispro de la concentración U200 no supera el precio por unidad de insulina lispro de concentración U100.
(4) Insulina glargina U300: solamente en personas con DM1 si el precio por unidad de insulina glargina de la concentración U300 no supera el precio por unidad de insulina glargina de concentración U100.
(5) Insulina degludec: personas con DM1 que presenten hipoglucemia nocturna con insulina glargina y/o detemir, habiéndose evaluado previamente: técnica de inyección, sitios de inyección, habilidades de autocontrol, conocimiento y habilidades de autogestión, estilo de vida, dificultades psicológicas y psicosociales, posibles causas orgánicas como la gastroparesia.
Deberán presentar la indicación acompañada de un resumen de historia clínica del médico especializado que incluya el registro de las hipoglucemias y la evaluación de los criterios mencionados previamente.
(6) Situaciones especiales: tratamiento intensificado con riesgo frecuente de hipoglucemias o bomba de insulina o gestantes con diabetes pregestacional o gestacional con insulina o mujer con diabetes que planifica su embarazo.
(7) Bomba de infusión: ante indicación expresa y fundamentada de profesional especializado, su otorgamiento deberá ser evaluado y aprobado por la auditoría de la institución que corresponda, utilizando como referencia las normas que al respecto ha establecido la Sociedad Argentina de Diabetes y que formarán parte del Programa Nacional de Garantía de Calidad de Atención Médica. Su prescripción no puede efectuarse por nombre comercial.
(8) Prescripción médica especializada: Médicos especialistas en Endocrinología y/o Nutrición, y aquellos especialistas en Clínica Médica, Medicina General y Pediatría, que acrediten capacitación en Diabetes (Especialización Universitaria a través de carreras de especialización y/o maestrías, capacitación en sociedades científicas afines) y un mínimo de cinco años de trabajo en un Servicio acreditado donde se traten pacientes con esta patología.
(9) Glucagón: Glucagón 1mg en personas con diagnóstico de DM1. Uno por año. Se autorizará la cobertura del glucagón más de una vez al año si la persona con DM1 confirma su utilización a través de resumen de historia clínica del profesional tratante.
(10) Vildagliptina- Sitagliptina (gliptinas o IDPP-4):
1. En personas adultas con DM2 como tratamiento complementario de la metformina cuando la persona presente todos estos criterios simultáneamente:
- No se logra la meta de HbA1c con dosis máxima tolerada de metformina (con 3 a 6 meses de tratamiento documentado).
- No presente contraindicaciones para la utilización de IDPP-4
- Los valores de HbA1 c no superen en más de un 1 % el valor meta
- Presentan riesgo aumentado de hipoglucemia.
2. En personas adultas con DM2 como tratamiento alternativo a la metformina cuando la persona presente todos estos criterios simultáneamente:
- Contraindicaciones para el uso de la metformina
- No tenga contraindicaciones para la utilización de IDPP-4
- Sus valores de HbA1 c no superen en más de un 1 % el valor meta.
- Presenten riesgo aumentado de hipoglucemia
(11) Glibenclamida: Basado en la evidencia actualmente disponible y las guías de práctica clínica que NO recomiendan el tratamiento con glibenclamida, se DISCONTINUA la cobertura 100% de Glibenclamida.
Se mantendrá la cobertura actual de glibenclamida por 6 meses a partir de la publicación del presente en el Boletín Oficial.
(12) La prescripción de los reflectómetros no podrá efectuarse por nombre comercial.
PROCEDIMIENTOS PROPUESTOS PARA EL SUMINISTRO DE MEDICAMENTOS Y OTROS INSUMOS
Los agentes del seguro de salud establecerán los procedimientos administrativos necesarios a fin de garantizar la provisión de medicamentos e insumos de la presente norma a las personas con diabetes comprendidas en dichos subsistemas. Para aquellas no pertenecientes a los agentes del seguro de salud, cada jurisdicción provincial y la ciudad autónoma de Buenos Aires podrá instrumentar los mecanismos necesarios teniendo en cuenta el domicilio de la persona con diabetes, el diagnóstico con certificado médico otorgado por establecimiento público o servicio asistencial estatal en que tendrá que estar registrado y al cual concurriría para control y tratamiento. Dicho procedimiento estará a cargo de profesionales habilitados por la autoridad competente. Dicho certificado deberá contener los datos correspondientes al formulario de acreditación para personas con diabetes. (Anexo II)
Las modificaciones a la norma precedente contenidas en este reglamento están basadas en una búsqueda exhaustiva, selección y análisis crítico de la evidencia proveniente de Guías de Práctica Clínica, revisiones sistemáticas y meta-análisis de alta calidad metodológica referentes a la temática, valorando especialmente la efectividad clínica y seguridad de las personas con diabetes.
Glosario
DM1: diabetes mellitus tipo 1
DM2: diabetes mellitus tipo 2
HbA1c: hemoglobina glicosilada A1c
IDPP4: inhibidores de la dipeptidil peptidasa 4
NPH: Neutral Protamine Hagedorn.
Aspectos relevantes de la actualización:
- Discontinuar la cobertura 100% de glibenclamida.
- Incorporar la cobertura de gliclazida.
- Excluir la cobertura de las Insulinas porcina y bovina, jeringas de insulina U40 y U80.
- Aumentar la cobertura del número de agujas para aplicación de insulina.
- Incorporar la cobertura de vildagliptina/sitagliptina, para subpoblaciones específicas.
- Incorporar la cobertura de insulinas lispro U200, glargina U300 y degludec para subpoblaciones específicas.
- Incorporar la cobertura de glucagón, para subpoblación especifica.
(1) Cantidades de referencia: son aquellas establecidas para dar respuesta adecuada a la gran mayoría de las personas con diabetes en los diferentes esquemas terapéuticos recomendados. Pueden ser modificadas ante casos particulares debidamente documentados mediante historia clínica y registro semanal de glucemias.
(2) Tratamiento intensificado: consiste en administración de insulina basal (NPH dos a tres veces al día, insulina detemir dos veces al día o insulina glargina/degludec, una vez al día), más insulina adicional de acción rápida en relación a las ingestas (insulina regular o análogos rápidos), o bomba de infusión continua subcutánea. El tratamiento intensificado será indicado por médico especializado (8).
(3) Insulina lispro U200: solamente si el precio por unidad de insulina lispro de la concentración U200 no supera el precio por unidad de insulina lispro de concentración U100.
(4) Insulina glargina U300: solamente en personas con DM1 si el precio por unidad de insulina glargina de la concentración U300 no supera el precio por unidad de insulina glargina de concentración U100.
(5) Insulina degludec: personas con DM1 que presenten hipoglucemia nocturna con insulina glargina y/o detemir, habiéndose evaluado previamente: técnica de inyección, sitios de inyección, habilidades de autocontrol, conocimiento y habilidades de autogestión, estilo de vida, dificultades psicológicas y psicosociales, posibles causas orgánicas como la gastroparesia.
Deberán presentar la indicación acompañada de un resumen de historia clínica del médico especializado que incluya el registro de las hipoglucemias y la evaluación de los criterios mencionados previamente.
(6) Situaciones especiales: tratamiento intensificado con riesgo frecuente de hipoglucemias o bomba de insulina o gestantes con diabetes pregestacional o gestacional con insulina o mujer con diabetes que planifica su embarazo.
(7) Bomba de infusión: ante indicación expresa y fundamentada de profesional especializado, su otorgamiento deberá ser evaluado y aprobado por la auditoría de la institución que corresponda, utilizando como referencia las normas que al respecto ha establecido la Sociedad Argentina de Diabetes y que formarán parte del Programa Nacional de Garantía de Calidad de Atención Médica. Su prescripción no puede efectuarse por nombre comercial.
(8) Prescripción médica especializada: Médicos especialistas en Endocrinología y/o Nutrición, y aquellos especialistas en Clínica Médica, Medicina General y Pediatría, que acrediten capacitación en Diabetes (Especialización Universitaria a través de carreras de especialización y/o maestrías, capacitación en sociedades científicas afines) y un mínimo de cinco años de trabajo en un Servicio acreditado donde se traten pacientes con esta patología.
(9) Glucagón: Glucagón 1mg en personas con diagnóstico de DM1. Uno por año. Se autorizará la cobertura del glucagón más de una vez al año si la persona con DM1 confirma su utilización a través de resumen de historia clínica del profesional tratante.
(10) Vildagliptina- Sitagliptina (gliptinas o IDPP-4):
1. En personas adultas con DM2 como tratamiento complementario de la metformina cuando la persona presente todos estos criterios simultáneamente:
- No se logra la meta de HbA1c con dosis máxima tolerada de metformina (con 3 a 6 meses de tratamiento documentado).
- No presente contraindicaciones para la utilización de IDPP-4
- Los valores de HbA1 c no superen en más de un 1 % el valor meta
- Presentan riesgo aumentado de hipoglucemia.
2. En personas adultas con DM2 como tratamiento alternativo a la metformina cuando la persona presente todos estos criterios simultáneamente:
- Contraindicaciones para el uso de la metformina
- No tenga contraindicaciones para la utilización de IDPP-4
- Sus valores de HbA1 c no superen en más de un 1 % el valor meta.
- Presenten riesgo aumentado de hipoglucemia
(11) Glibenclamida: Basado en la evidencia actualmente disponible y las guías de práctica clínica que NO recomiendan el tratamiento con glibenclamida, se DISCONTINUA la cobertura 100% de Glibenclamida.
Se mantendrá la cobertura actual de glibenclamida por 6 meses a partir de la publicación del presente en el Boletín Oficial.
(12) La prescripción de los reflectómetros no podrá efectuarse por nombre comercial.
PROCEDIMIENTOS PROPUESTOS PARA EL SUMINISTRO DE MEDICAMENTOS Y OTROS INSUMOS
Los agentes del seguro de salud establecerán los procedimientos administrativos necesarios a fin de garantizar la provisión de medicamentos e insumos de la presente norma a las personas con diabetes comprendidas en dichos subsistemas. Para aquellas no pertenecientes a los agentes del seguro de salud, cada jurisdicción provincial y la ciudad autónoma de Buenos Aires podrá instrumentar los mecanismos necesarios teniendo en cuenta el domicilio de la persona con diabetes, el diagnóstico con certificado médico otorgado por establecimiento público o servicio asistencial estatal en que tendrá que estar registrado y al cual concurriría para control y tratamiento. Dicho procedimiento estará a cargo de profesionales habilitados por la autoridad competente. Dicho certificado deberá contener los datos correspondientes al formulario de acreditación para personas con diabetes. (Anexo II)
ANEXO II:
(Anexo rectificado por art. 2° de la Resolución N° 764/2018 de la Secretaría de Gobierno de Salud B.O. 12/12/2018)